氧化还原反应
【考点梳理】
1、氧化还原反应的特征(判断方法): _____________________________。
2、氧化还原反应的实质:电子的转移或得失。
3、氧化还原反应中各相关概念间的关系:
______电子,价______,被______(发生______反应),______剂(具有______性);
______电子,价______,被______(发生______反应),______剂(具有______性)。
4、氧化还原反应的表示方法:
(1)双线桥法:表示氧化剂、还原剂得失电子的结果。
注意:①箭头必须由反应物指向生成物,起始为不同价态的同种元素;
②在“桥”上标明电子得失数目,且电子电子总数相等。如:
Cl2+2KI=2KCl+I2
(2)单线桥法:表示电子转移的方向和数目。
注意:①箭头起点为失电子元素,终点为得电子元素;
②只标转移电子总数,不写“得”与“失”。如:
Cl2+2KI=2KCl+I2
【体验真题】
1.(2009-16)2008年我国的“神舟七号”宇宙飞船搭载3名宇航员顺利升空,并成功实现宇航员太空行走。火箭和飞船升空所需的巨大能量可由下列化学反应提供:
C2H8N2+2N2O4==2CO2↑+3N2↑+4H2O
有关该反应的说法正确的是( )
A.该反应是分解反应 B.反应中碳元素的化合价降低
C.氧化剂是N2O4 D.该反应不是氧化还原反应
2.(2010-16)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。下列反应可制取K2FeO4:
2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6KCl+8H2O
2K2FeO4+6KCl+8H2O
对于该反应,下列说法正确的是( )
A.该反应是置换反应 B.钾元素化合价降低
C.Fe(OH)3发生还原反应 D.Cl2是氧化剂
3.(2011-17)制太阳能电池需要高纯硅,工业上用粗硅制高纯硅可通过以下反应实现:
①Si+3HCl(气)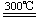 SiHCl3(气)+H2 ②SiHCl3(气)+H2
SiHCl3(气)+H2 ②SiHCl3(气)+H2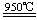 Si+3HCl(气)
Si+3HCl(气)
对上述两个反应的叙述错误的是( )
A.都是置换反应 B.都是氧化还原反应
C.反应中硅元素都被还原 D.都不是离子反应
4.(2012-11)高铁的快速发展方便了人们的出行。工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:2Al+Fe2O3 2Fe+Al2O3,其中Fe2O3是( )
2Fe+Al2O3,其中Fe2O3是( )
 A.氧化剂 B.还原剂
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
5.(2013-18)反应2NO+2CO N2+2CO2应用于汽车尾气的净化。下列判断正确的( )
N2+2CO2应用于汽车尾气的净化。下列判断正确的( )
A.该反应是置换反应 B.该反应是复分解反应
C.CO是氧化剂 D.NO发生还原反应
6.(2014-15)我国古代就有湿法炼铜的记载“曾青得铁则化为铜”,反应为Fe+CuSO4=Cu+FeSO4。有关该反应的说法正确的是( )
A.Fe是氧化剂 B.CuSO4是还原剂 C.Fe被氧化 D.CuSO4发生氧化反应
7、(2015-17)中国最新战机歼-31使用了高强度、耐高温的钛合金材料。工业上冶炼钛的反应如下:TiCl4+2Mg  Ti+2MgCl2。下列有关该反应的说法正确的是
Ti+2MgCl2。下列有关该反应的说法正确的是
A.TiCl4是还原剂 B.Mg被氧化
C.TiCl4发生氧化反应 D.Mg得到电子
【应对策略】必考题型和知识点,并呈现起点高落点低的特点,学生多有畏难现象。做到两点难点可化解:①能正确标出元素化合价,并找到变价元素;
②串好两条主线,即 “失—升—氧化—还原剂”、“得—降—还原—氧化剂”。③电子转移的表示方法:双线桥和单线桥。
